Abstrak
Janji pendaran terpolarisasi sirkuler yang ditingkatkan (CPL) dari molekul organik telah mengilhami upaya sintetis untuk menyiapkan helicena multilapis yang memanjang. Telah terbukti sangat menantang untuk mensintesis dan mengisolasi helicena multiputaran yang murni secara enantiomerik, dan akibatnya, pedoman yang jelas untuk desain molekuler helicena untuk mencapai keluaran CPL yang besar masih sulit dipahami. Kami mengeksplorasi dimerisasi oksidatif dari hetero[13]helicena yang dianol 2-naftol, dan mengamati pembentukan dua jenis hetero[27]helicena yang secara struktural berbeda, keduanya dengan empat putaran heliks. Dengan Cu II Cl(OH)-TMEDA sebagai oksidan, dimer simetris ( bi[13] ) terbentuk, menggabungkan dua helicena dengan helisitas yang sama dalam bentuk keto tautomeriknya. Penggunaan Cu II (OTf)₂ sebagai oksidan menghasilkan [27]helicenoid tak simetris yang tersusun dari enantiomer ( M ) dan ( P ) dari [13]helicena melalui penggabungan tak biasa antara posisi 1 dan 3 dari unit 2-naftol. Karakterisasi struktur dicapai dengan spektroskopi NMR dan analisis difraksi kristal tunggal (sinar-X atau elektron). Enantiomer dari [27]helicenoid ini dianalisis dengan pengukuran dikroisme sirkuler elektronik (ECD) dan CPL. Data spektroskopi diperkuat oleh perhitungan DFT, dan keluaran CPL intens dipertahankan meskipun terdapat helicena ( M ) dan ( P ) dalam molekul yang sama. [27]helicenoid ini adalah struktur terisolasi pertama yang memiliki sistem π heliks dengan empat lilitan heliks.
Perkenalan
Helisena adalah molekul yang sepenuhnya terkonjugasi, berfusi orto yang bersifat kiral karena kendala konformasi. [ 1 – 6 ] Kiralitas heliks dan sifat-sifat kiroptis unik yang terkait, seperti dikroisme sirkuler elektronik (ECD) dan pendaran terpolarisasi sirkuler (CPL), membuat helisena menarik untuk aplikasi dalam CLP-OLED. [ 7 – 14 ] Pengamatan baru-baru ini menunjukkan bahwa helisena yang memanjang dan struktur heliks lainnya dapat menyebabkan amplifikasi asimetri yang kuat, yang berpotensi meningkatkan sifat-sifat kiroptis dalam molekul-molekul ini. [ 15 – 17 ] Fenomena ini telah memacu minat yang signifikan dalam sintesis molekul dan bahan kiral heliks yang lebih panjang selama beberapa dekade terakhir. [ 15 , 18 – 20 ] Arsitektur seperti helisena polimerik, seperti pita nano graphene yang melingkar secara heliks, juga telah muncul sebagai pendekatan yang menjanjikan untuk memperkuat sifat-sifat kiroptis dan magnetik, seperti yang ditunjukkan dalam penelitian baru-baru ini. [ 21 – 23 ] Namun, berdasarkan literatur eksperimental terkini bagaimana respons kiroptikal helicena, khususnya intensitas ECD dan CPL, berskala dengan penambahan lilitan heliks dalam deret homolog. [ 24 ] Studi komputasional menunjukkan bahwa respons ECD setelah pemanjangan karbo[ n ]helicena hingga n = 30 cincin benzena didominasi oleh transisi berenergi rendah ketika n lebih besar dari 12, yang sesuai dengan kira-kira dua lilitan heliks. [ 25 ] Dalam penelitian terkini bersama dengan kelompok Nuckolls dan Santoro, kami menunjukkan amplifikasi lebih dari linier dari keluaran ECD dan CPL ( g lum ) dalam helicena perylene diimide (PDI) yang memanjang seiring bertambahnya panjangnya. [ 26 ]
Amplifikasi g lum [ 27 ] dan kecerahan fluoresensi ( B lum ) [ 28 ] ini merupakan hasil dari penyelarasan progresif vektor momen dipol transisi magnetik (| m |) dan listrik (| μ |), seiring dengan perpanjangan tulang punggung heliks. Hasil-hasil ini menunjukkan bahwa sintesis helicena yang lebih panjang dapat lebih memperkuat efek kiroptikal. Sementara struktur dengan satu hingga tiga putaran heliks telah dilaporkan (Gambar 1a ), [ 29 – 33 ] pembuatan helicena multi-putaran tetap menjadi tantangan sintetis utama yang ingin kami atasi dalam penelitian ini.
Gambar 1
Buka di penampil gambar
Kekuatan Gambar
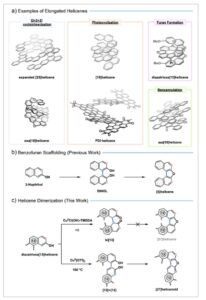
a) Pilihan helicena memanjang π, dan metodologi sintesis utama yang digunakan untuk mensintesisnya. [ 29 – 34 ] b) Strategi perancah benzofuran diilustrasikan oleh oksidasi 2-naftol menjadi BINOL diikuti oleh reaksi dehidrasi untuk menghasilkan [5]helicena. [ 35 ] c) Helicenoid yang tidak biasa ( bi[13] dan [27]helicenoid ) dijelaskan dalam karya ini. Konektivitas dalam perancah benzofuran disorot.
Bahasa Indonesia: Dalam pekerjaan kami sebelumnya, kami mengeksplorasi strategi perancah benzofuran untuk memanjangkan helicena, yang telah terbukti menjadi transformasi yang kuat dalam perjalanan menuju helicena yang berbeda seperti berbagai diazadioxa[13]helicena berlapis dua. [ 31 ] Strategi ini mudah: pertama, kopling oksidatif C–C pada posisi orto dari dua fenol menghubungkan fragmen helicena, diikuti oleh dehidrasi yang dimediasi asam untuk membentuk cincin furan (Gambar 1b ). Kami bertujuan untuk lebih memperluas metodologi sintetis ini untuk menyiapkan helicena yang lebih panjang dengan dimerisasi diazadioxa[13]helicena diikuti oleh pembentukan cincin furan. Di sini, kami mengamati reaktivitas yang tidak terduga dalam gugus 2-naftol yang dianulasi, yaitu kopling antara posisi-1 dari satu 2-naftol dan posisi-3 dari gugus 2-naftol lainnya ( [27]helicenoid , Gambar 1c ). Kami juga mengamati penjebakan sistem BINOL π-extended dalam konfigurasi di-keto ( bi[13] Gambar 1c ).
Hasil dan Pembahasan
Sintesis
Kami menyiapkan helicena HO[13]OMe menurut protokol yang dipublikasikan sebelumnya. [ 31 ] Perpanjangan tulang punggung helicena dengan pendekatan perancah benzofuran dengan turunan 2-naftol terbukti menantang. Kami memfokuskan upaya kami pada pembentukan benzofuran dengan dimerisasi [13]helicena diikuti oleh dehidrasi. Kami segera menyadari bahwa produk yang berbeda terbentuk ketika menerapkan strategi dimerisasi. Pembentukan produk bergantung pada apakah campuran rasemat dari ( M ) – dan ( P ) -helicena atau helicena enantiopure (baik ( M ) – atau ( P ) -helicena) digunakan, dan juga pada kondisi reaksi yang diterapkan (Skema 1 ). Bahasa Indonesia: Ketika [13]helicena murni enantiomerik digunakan sebagai bahan awal dalam kombinasi dengan Cu II Cl(OH)-TMEDA (TMEDA = tetramethylethylendiamine) sebagai oksidan, pembentukan dimer 1,4-diketon bi[13] diamati bukannya dimer 1,4-πdiol seperti yang diharapkan (Skema 1a ). [ 36 ] Perilaku fenol yang tidak biasa untuk menghasilkan 1,4-diketon bukan sepenuhnya tanpa preseden, karena motif serupa telah diamati oleh Shinokubo dan rekan kerja ketika mendimerisasi 2-hidroksi antrasena yang difungsionalisasi. [ 36 ] Ketika [13]helicena rasemat digunakan, bi[13] tetap menjadi produk utama. Menundukkan bi[13] pada kondisi reaksi asam yang biasanya digunakan untuk membentuk cincin furan—dan dengan itu [27]helicena—menyebabkan pengembalian dimer bi[13] kembali ke bahan awal. Pembalikan bi[13] menjadi HO[13]OMe adalah transformasi tidak biasa lainnya karena tidak ada penjelasan mekanistik yang jelas, namun Tanaka dan rekan-rekannya telah mengamati reaksi serupa dalam upaya untuk mendimerisasi helicena yang mengandung pirol kiral. [ 37 ] Mereka mengamati bahwa pembalikan menjadi monomer juga dapat dimediasi dengan cahaya, tetapi mereka tidak mengomentari sumber agen pereduksi atau sumber atom hidrogen tambahan yang dibutuhkan. Dalam reaksi kami, suhu tinggi menyebabkan dekomposisi menjadi campuran produk yang tidak teridentifikasi. Perlakuan dengan basa juga mengakibatkan dekomposisi, dan karenanya juga bukan rute yang layak menuju [27]helicena. Di bawah kondisi reaksi ini, rangkaian percobaan ini menyoroti perilaku narsistik reaksi, di mana ( M ) -helicena berpasangan secara eksklusif dengan ( M ) -helicena dan( P ) -helicenes berpasangan secara eksklusif dengan ( P ) -helicenes. Struktur bi[13] menyajikan contoh bentuk naftol-keto yang diperpanjang secara signifikan π, dan keberadaan konfigurasi struktural ini menyoroti tantangan pembentukan sistem π yang tegang, seperti helicenes yang diperpanjang.
Skema 1
Buka di penampil gambar
Kekuatan Gambar
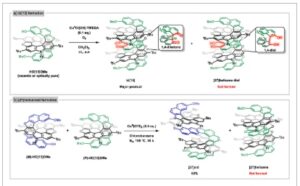
a) Sintesis struktur helicenoid empat lapis bi[13] diketon melalui dimerisasi stereoselektif dari [13]helicena ( M ) – atau ( P ) -. b) Sintesis [27]helicenoid melalui dimerisasi [13]helicena ( M ) – dan ( P ) – dengan penggandengan oksidatif antara posisi 1 dan 3 dari unit 2-naftol.
Bahasa Indonesia: Ketika campuran rasemat helicena HO[13]OMe diperlakukan dengan Cu II (OTf) 2 (Skema 1b ), produk benzofuran dideteksi dengan spektrometri massa resolusi tinggi (HRMS). Yang mengejutkan kami, produk fluoresensi biru kuat yang diisolasi telah kehilangan simetrinya, seperti yang diamati dengan menganalisis spektrum 1H NMR. Faktanya, reaksi penggandengan oksidatif langsung selektif antara posisi 1 dan 3ʹ dari dua helicena dengan helisitas berlawanan telah terjadi ( [27]helicenoid ). Ini mengejutkan karena sejumlah alasan. Pengamatan penggandengan pada posisi 3 dari 2-naftol belum pernah terjadi sebelumnya, dan reaktivitas homokiral yang diamati dalam reaksi yang dimediasi Cu II Cl(OH)-TMEDA terbalik. Di sisi lain, struktur tersebut memperoleh daerah aromatik yang hampir planar yang lebih besar, yang mungkin merupakan gaya pendorong. Dehidrasi tidak diamati di bawah 100 °C; Namun, pada suhu tinggi ini, reaksi berlanjut hingga membentuk cincin furan, yang menghasilkan pembentukan produk seperti helicena dengan hasil isolasi sebesar 58%.
Analisis struktural
Senyawa bi[13] ditemukan tidak stabil selama pemurnian kromatografi, sebagian besar kembali ke bahan awal, HO[13]OMe . Akibatnya, karakterisasi spektroskopi NMR dilakukan pada campuran reaksi mentah setelah pengerjaan tetapi sebelum (apa pun) pemisahan kromatografi (lihat Informasi Pendukung; Gambar S4 ).
Dengan mengamati spektrum NMR HSQC 1 H– 13 C bi[13] mentah dalam CD 2 Cl 2 , C hibridisasi sp 3 dideteksi pada 57,0 ppm (Gambar S7 ) dengan proton terkait pada 2,63 ppm (Gambar S5 ). Kami juga mengamati sinyal karbonil keton yang jelas dalam spektrum NMR APT64 pada 191,40 ppm (Gambar S6 ) dan pembentukan bi[13] didukung oleh HRMS (Gambar S25, S26 ). Struktur tiga dimensi senyawa bi[13] ditentukan dengan difraksi sinar-X (XRD). Kristal tunggal berbentuk jarum kuning diperoleh dengan difusi lambat etanol ke dalam larutan CH 2 Cl 2 pada suhu kamar. Data kristalografi untuk bi[13] murni optik dilaporkan dalam Tabel S1 dan unit asimetris yang diamati dalam struktur kristal ditunjukkan pada Gambar 2a . Struktur yang ditunjukkan di sini adalah dimer dari dua [13]helicene dengan ( P )-helicity. Sejauh pengetahuan kami, ini adalah helicene pertama yang dilaporkan yang menampilkan sistem π empat lapis. Heliks bi[13] panjangnya ∼1,2 nm dan ikatan tunggal C–C yang menghubungkan dua unit [13]helicene panjangnya 1,625(7) Å, yang jauh lebih panjang daripada heliks umum.mathematical equationikatan (1,54 Å). [ 38 ] Ikatan yang memanjang ini bisa menjadi salah satu faktor penyebab ketidakstabilan bi[13] ketika mengalami kondisi reaksi apapun, karena pemanjangan ini akan melemahkan ikatan, sehingga lebih mudah putus.
Gambar 2
Buka di penampil gambar
Kekuatan Gambar
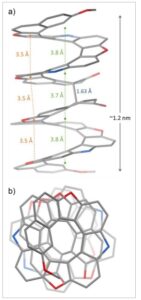
a) Struktur molekul sederhana dari ( P )- bi[13] . Jarak rata-rata antara putaran berurutan dilaporkan dalam warna hijau, sedangkan jarak susun terdekat, yang ditemukan antara cincin furan, ditunjukkan dalam warna oranye. Nilai dalam warna biru mengacu pada ikatan tunggal C–C di bagian tengah. Kode warna: C = abu-abu, O = merah, N = biru. Gugus alkil dan atom hidrogen dihilangkan demi kejelasan. Lihat Informasi Pendukung untuk metode pengukuran jarak. b) Molekul yang sama dilihat sepanjang sumbu heliks, menunjukkan empat putaran.
Bukti pertama pembentukan [27]helicenoid adalah analisis HRMS (Gambar S23, S24 ). Analisis spektrum 1H NMR lebih lanjut dari [27]helicenoid mengungkapkan 26 proton aromatik, dua sinyal metoksi yang berbeda dan delapan sinyal t -butil, yang membuktikan struktur [27]helicenoid yang tidak simetris (Gambar S5 ). Kristal [27]helicenoid tumbuh dengan penguapan lambat larutan CH2Cl2 dan etanol dari rasemat [27]helicenoid untuk menghasilkan jarum kuning berukuran beberapa mikron. Namun, kristal ini tidak cocok untuk analisis XRD kristal tunggal. Sebaliknya, mereka terbukti cocok untuk pengukuran difraksi elektron (ED) (Tabel S1 ). [ 39 ]
Senyawa tersebut menunjukkan beberapa polimorfisme (lihat Informasi Pendukung untuk rincian lebih lanjut). Struktur kristal dipecahkan dalam grup ruang ortorombik Pna 2 1 yang menunjukkan dua molekul independen per unit asimetris (Gambar S1 ). [27]helicenoid menampilkan enantiomer ( M ) dan ( P ) dari prekursor [13]helicena, dan enantiomer ( MP ) dan ( PM ) dari [27]helicenoid hadir dalam struktur kristal, dengan total 8 molekul dalam sel satuan. Pengepakan kristal tidak menampilkan interaksi π···π intermolekul dan agak longgar, menyisakan sekitar 12% volume rongga dalam sel satuan. [ 39 ] Struktur keadaan padat dari [27]helicenoid adalah contoh pertama dari heterohelicena terkonjugasi penuh berlapis empat (Gambar 3 ). Pitch heliks berada di sekitar 3,6–3,7 Å (Gambar S2 ), yaitu, sedikit lebih longgar dibandingkan dengan prekursor [13]helicene (3,5 Å, lihat Informasi Pendukung). Jarak antar-planar cincin demi cincin bervariasi dengan lancar di sepanjang heliks dan minimal di antara cincin furan (3,4–3,5 Å, Gambar S3 ), yang menunjukkan interaksi π···π antarlapisan yang menguntungkan, [ 40 ] terlepas dari struktur yang sangat tegang.
Gambar 3
Buka di penampil gambar
Kekuatan Gambar
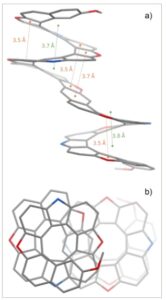
a) Struktur molekul sederhana dari ( PM )- [27]helicenoid . Jarak rata-rata antara putaran berurutan dilaporkan dalam warna hijau, sedangkan jarak susun terdekat, yang melibatkan cincin furan, ditunjukkan dalam warna oranye. Kode warna: C = abu-abu, O = merah, N = biru. Gugus alkil dan atom hidrogen dihilangkan demi kejelasan. Lihat Informasi Pendukung untuk metode pengukuran jarak. b) Molekul yang sama dilihat sepanjang sumbu heliks, menunjukkan heliks yang terhuyung-huyung dengan kiralitas yang berlawanan.
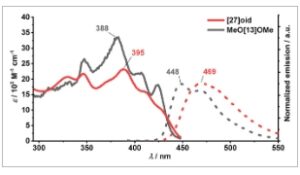
Sifat penyerapan dan emisi . Spektrum penyerapan UV–vis dan fluoresensi [27]helicenoid diukur dalam CH 2 Cl 2 pada suhu kamar dan dibandingkan dengan spektrum MeO[13]OMe yang dilaporkan sebelumnya (Gambar 4 dan S9, S10 ). [27]Helicenoid menunjukkan koefisien penyerapan molar yang berkurang hingga 30% dibandingkan dengan [13]helicena ( ε max ≈ 33.500 untuk MeO[13]OMe versus ε max ≈ 23.000 M −1 cm −1 untuk [27]helicenoid ). Ketika membandingkan spektrum penyerapan MeO[13]OMe dan [27]helicenoid , perkembangan vibronik keduanya sangat mirip. Perbedaan utama dalam spektrum serapan adalah pergeseran merah kecil sebesar 460 cm −1 dari transisi elektronik terkuat dalam spektrum tampak, yang bergerak dari MeO[13]OMe ke [27]helicenoid . Tepi pita serapan hampir identik untuk kedua spesies. Pengamatan luar biasa bahwa spektrum serapan hampir tidak terpengaruh setelah menggandakan jumlah unit aromatik dalam sistem, menunjukkan bahwa panjang konjugasi efektif (ECL) dalam sistem ini telah mencapai batasnya. Ini juga dapat dilihat dengan memeriksa orbital transisi alami (NTO, Gambar S16 ) karena beberapa transisi pertama terlokalisasi dalam satu unit [13]helicena, yang hanya meluas ke bagian naftol dari [13]helicena kedua. Ketika membandingkan spektrum emisi kedua spesies ini, pergeseran merah kecil sebesar 1000 cm −1 diamati. Bahasa Indonesia: Setelah dimerisasi, hasil kuantum fluoresensi, ϕ fl telah hampir berkurang setengahnya (0,18 untuk [27]helicenoid versus 0,28 untuk MeO[13]OMe ), yang menunjukkan jalur peluruhan non-radiatif baru yang diperkenalkan dalam dimer annulated. Pemeriksaan orbital transisi alami (NTO, Gambar S16 ) dari dua transisi elektronik pertama dalam [27]helicenoid menunjukkan bahwa S 0 → S 1 dan S 0 → S 2 terlokalisasi dalam unit [13]helicena, hanya meluas ke bagian naftol dari [13]helicena kedua. Ini bisa menjadi alasan mengapa spektrum serapan hanya berubah sedikit untuk [27]helicenoid .
Gambar 4
Buka di penampil gambar
Kekuatan Gambar
Spektrum serapan dan emisi [27]helicenoid dan MeO[13]OMe terekam dalam CH 2 Cl 2 . Spektrum serapan direpresentasikan dengan garis utuh dan emisi direpresentasikan dengan garis putus-putus.
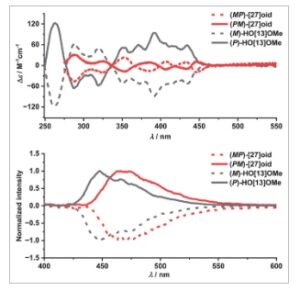
Sifat kiroptis . Dua enantiomer [27]helicenoid berhasil dipisahkan dengan HPLC pada fase stasioner kiral (untuk detailnya, lihat Informasi Pendukung, Gambar S8 ) untuk menyelidiki sifat kiroptisnya dan membandingkannya dengan bahan awal HO[13]OMe . Seperti yang ditunjukkan pada Gambar 5 (atas), spektrum ECD dari fraksi pertama dan kedua yang direkam dalam CH2Cl2 mengungkapkan hubungan bayangan cermin yang sempurna. Enantiomer pertama yang dielusi HPLC menunjukkan efek Cotton positif-ke-negatif.
Gambar 5
Buka di penampil gambar
Kekuatan Gambar
Spektrum ECD (atas) dan CPL (bawah) dari HO[13]OMe (hitam) dan [27]helicenoid (merah) dalam CH 2 Cl 2 pada suhu kamar.
Puncak bayangan cermin diamati untuk enantiomer elusi kedua. Konfigurasi absolutnya ditetapkan dengan membandingkan ECD eksperimental dengan spektrum ECD yang disimulasikan TDDFT (Gambar S15 ). Dengan demikian, fraksi pertama dan kedua masing-masing sesuai dengan enantiomer ( PM ) – dan ( MP ) . Pita ECD terkuat dari [27]helicenoid ( Δε ∼ 40 M −1 cm −1 ) diamati di wilayah UV sementara pita terkuat ( Δε ∼ 20 M −1 cm −1 ) di bagian spektrum tampak terletak tepat di atas 350 nm. Ini adalah penurunan signifikan dari HO[13]OMe . Spektrum ECD dari kedua enantiomer [27]helicenoid menunjukkan efek Cotton positif dan negatif bergantian di atas 330 nm, berbeda dengan HO[13]OMe , di mana pita di atas ambang ini secara seragam positif atau negatif. Pola ini kemungkinan merupakan hasil dari kombinasi heliksitas ( P )- dan ( M )- dalam [27]helicenoid , yang berkontribusi pada efek Cotton yang berlawanan dan berpotensi mengurangi absorbansi cahaya terpolarisasi melingkar. Enantiomer [27]helicenoid menampilkan spektrum CPL bayangan cermin dalam CH 2 Cl 2 (Gambar 5 , bawah dan Gambar S11, S12 ). Nilai glum sebesar 5,5 × 10 −3 tercatat untuk [27]helicenoid pada 469 nm dan untuk HO[13]OMe, glum sebesar 4,2 × 10 −3 pada 448 nm, yang berada pada orde besaran yang sama dengan yang diamati untuk aza- dan heterohelicena lainnya . [ 28 , 33 ]
Untuk mengetahui apakah perbedaan dalam sifat-sifat kiroptik ini unik pada peleburan dua gugus dengan heliksitas berlawanan dan motif struktur “kabel telepon”, atau hanya hasil dari pergeseran energi transisi akibat perluasan πsistem lebih lanjut, kami memodelkan struktur heliksenoida [27] yang disederhanakan dengan teori fungsi kerapatan. Teori fungsi kerapatan bergantung waktu (TD-DFT), yang mampu menangani keadaan elektronik tereksitasi, telah menjadi pendekatan mapan untuk memodelkan spektroskopi heliksena. [ 41 – 44 ]
Dalam struktur yang disederhanakan ini, kami mengganti gugus t -butil dan propil yang besar dengan gugus metil. Sebagai perbandingan, kami juga memodelkan struktur HO[13]OMe dengan dan tanpa struktur jembatan (furan), karena jembatan ini sendiri sudah memperluas gugus HO[13]OMe asli . Pembahasan terperinci tentang hasil komputasi dapat ditemukan di Informasi Pendukung (Gambar S13–S16 dan Tabel S2, S3 ).
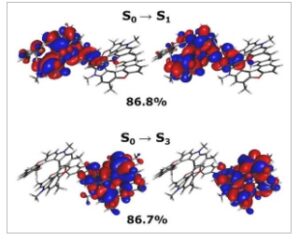
Baik struktur “kabel telepon” dan perpanjangan sistem berkontribusi pada struktur kompleks spektrum ECD dari [27]helicenoid . Pertama, HO[13]OMe memperkenalkan serangkaian keadaan tereksitasi dengan rotasi optik yang berlawanan. Penambahan jembatan furan memperluas sistem π, menurunkan energi eksitasi transisi yang terlokalisasi pada bagian HO[13]OMe dari [27]helicenoid yang lebih baik digabungkan ke jembatan furan. Ini dimungkinkan karena jembatan furan tidak terhubung secara simetris dan karena itu akan mendukung delokalisasi ke salah satu sisinya. Stabilisasi ini tertinggi untuk transisi pertama, di mana ia berjumlah −0,10 eV. Ini juga dapat dilihat dari NTO (Gambar S16 ), di mana kerapatan elektronik bergeser ke area penjembatan, meskipun tidak melewatinya, menandakan pemutusan sistem π. Dari NTO [27]helicenoid yang digambarkan pada Gambar 6 , kita mengamati bahwa transisi elektronik berenergi terendah, tetap terlokalisasi pada salah satu bagian [27]helicenoid . Area penghubung terlibat dalam transisi, meskipun tidak melewatinya, menandakan adanya pemutusan pada sistem π.
Gambar 6
Buka di penampil gambar
Kekuatan Gambar
NTO dari dua transisi singlet elektronik pertama dalam struktur [27]helicenoid yang disederhanakan dan nomor pendudukannya. 90% kepadatan elektronik ditampilkan.
Ketika kedua gugus ( M ) dan ( P ) dijembatani bersama, simetrinya rusak dan kita melihat dua pola keadaan yang berlawanan dan saling bertautan, dipisahkan oleh energi stabilisasi yang disebutkan sebelumnya. Hasilnya adalah spektrum ECD yang berosilasi kuat, setidaknya di wilayah energi yang lebih rendah (dan kepadatan keadaan yang lebih rendah).
Kesimpulan
Dalam karya ini kami menggambarkan sintesis [27]helicenoid berlapis empat pertama. Dimulai dari campuran rasemat [13]helicena yang dijelaskan sebelumnya, kami berharap untuk memperoleh [27]helicena melalui reaksi dimerisasi/siklisasi [13]helicena yang dikatalisis tembaga. Anehnya, reaksi ini tidak menghasilkan [27]helicena yang ditargetkan melalui kopling C–C pada posisi 1,1′, tetapi malah mengarah pada pembentukan helicenoid analog, yang dibentuk oleh kopling C–C pada posisi 1,3′. [27 ]helicenoid yang dihasilkan menampilkan massa molekul yang sama dengan [27] , tetapi merupakan dimer heterokiral dari dua [13]helicena (yaitu, enantiomer ( M ) – dan ( P ) ). Fitur struktural dan sifat (kir)optik [27]helicenoid ditentukan dengan difraksi elektron, spektroskopi UV-vis, dan pengukuran ECD dan CPL. Untuk analisis terakhir, dua enantiomer rasemat [27]helicenoid berhasil dipisahkan. Didukung oleh studi TD-DFT, diamati bahwa [27]helicenoid mampu memutar cahaya terpolarisasi melingkar dari kiralitas ( M ) – dan ( P ) . Pengamatan ini juga dapat menjelaskan mengapa spektrum UV-vis [13]helicena dan [27]helicenoid terlihat sangat mirip. Kedua struktur tersebut memiliki sistem π empat lapis dengan empat lilitan heliks, yang merupakan sistem seperti helicena terpanjang yang dilaporkan.
![Helicena dengan Empat Lilitan Heliks: Dimerisasi [13]Helicena menjadi [27]Helicenoida](https://thefaheempro.com/wp-content/uploads/2025/05/image-2025-05-05T110611.535.jpg)